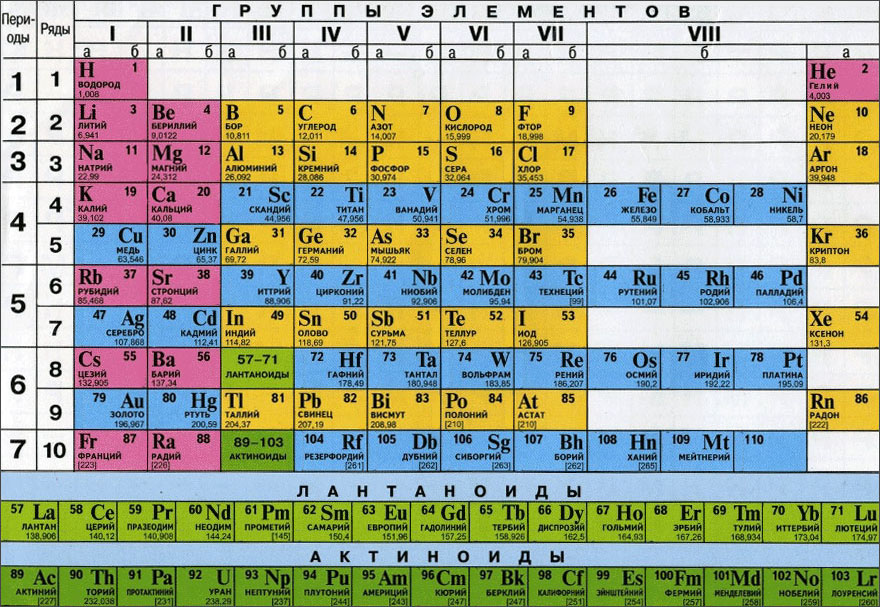
Периодическая система химических элементов — это таблица, в которой элементы систематизированы по возрастанию атомных номеров. Она является основой для изучения и понимания химии. Первой версией периодической системы была система Менделеева, разработанная в 1869 году русским химиком Дмитрием Ивановичем Менделеевым. В течение более ста лет периодическая система была усовершенствована и дополнена новыми открытиями в области химии.
Периодический закон Д. И. Менделеева утверждает, что свойства химических элементов периодически повторяются при упорядоченном расположении их в периодической системе. Свойства элементов, такие как атомные радиусы, ионообразование, электроотрицательность и тепловая активность, имеют периодическую зависимость от атомных номеров.
Благодаря периодическому закону Менделеева была предсказана существование ранее неизвестных элементов и проведены эксперименты для их открытия. Менделеев разместил элементы в таблице таким образом, чтобы элементы с схожими свойствами находились в одной вертикали — группе, а элементы с похожими электронными структурами были расположены в одной горизонтали — периоде.
Периодическая система химических элементов и периодический закон Менделеева играют важную роль в области химии и науки в целом. Они помогают исследователям классифицировать элементы, предсказывать их свойства и взаимодействия, а также понять основные закономерности природы и строение материи.
Периодическая система химических элементов
Периодическая система химических элементов – универсальная система классификации химических элементов, которая отражает их химические и физические свойства. Эта система была разработана русским химиком Дмитрием Ивановичем Менделеевым в 1869 году и с тех пор стала основой для изучения химии и химических процессов.
Периодическая система состоит из таблицы, в которой элементы разделены на строительные блоки, называемые периодами и группами. Периоды расположены горизонтально, а группы – вертикально. Всего в периодической системе 7 периодов и 18 групп.
Основные элементы периодической системы состоят из атомов, которые имеют определенное количество протонов в ядре и соответствуют определенному атомному номеру. Эти элементы классифицируются по своей химической активности и другим физическим свойствам.
В периодической системе элементы представлены символами, обозначающими их химические элементы:
- Главные группы обозначены числами от 1 до 18, начиная слева от таблицы.
- Первая главная группа представлена элементами с общей характеристикой – они образуют соединения с одним электроном во внешней оболочке.
- Вторая главная группа представлена элементами с общей характеристикой – они образуют соединения с двумя электронами во внешней оболочке.
- Таким образом, каждая главная группа имеет свою характеристику внешней оболочки элемента.
Периодическая система химических элементов имеет большое значение в науке и промышленности. Она позволяет упорядочить и систематизировать огромное количество химических элементов и предсказывать их химические свойства и реакции. Данная система также помогает в однозначной идентификации элементов и в создании новых материалов с определенными свойствами, что является основой для развития современных технологий и промышленности.
История создания
Периодическая система химических элементов была разработана русским химиком Дмитрием Ивановичем Менделеевым в 1869 году. Менделеев сформулировал периодический закон, основанный на анализе свойств химических элементов и их атомных масс. Он разместил элементы в таблице, называемой периодической системой, где они были упорядочены по возрастанию атомных масс.
Периодическая система Менделеева была революционным достижением в химии. Она представила упорядоченную структуру для классификации всех известных элементов и позволила предсказывать свойства еще не открытых элементов.
Система Менделеева оказалась крайне полезной в дальнейшем развитии химии. Она стала основой для проведения экспериментов, разработки новых соединений и поиска практических применений элементов. С течением времени периодическая система продолжала совершенствоваться и дополняться новыми открытиями в области химии и физики элементов.
Интересно отметить, что Менделеев предсказал существование элементов, которые были открыты позже. Он оставил пустые места в таблице для таких элементов и даже определил их свойства на основе свойств соседних элементов.
В настоящее время периодическая система химических элементов активно используется в химии, физике, биологии и других науках. Она помогает ученым понять основные закономерности в строении и свойствах элементов, а также служит основой для классификации новых открытий в области химии.
Открытие химических элементов
Одним из главных ученых, занимавшихся открытием химических элементов, был Дмитрий Иванович Менделеев. Он разработал периодическую систему элементов, которая стала основой для их классификации и открытия новых.
Первый химический элемент, который был открыт, это водород. Открытие водорода было делом не одного ученого, но многие источники считают, что это произошло в 1766 году двумя шведскими химиками Карлом Вилгельмом Шееле и Генрихом Кавендишем.
Однако большинство химических элементов было открыто впоследствии в XIX и XX веках. Многие из них были открыты Д. И. Менделеевым и другими учеными, работавшими в этой области.
- В 1807 году английский ученый Гамфри Дэви открыл элемент натрий.
- В 1808 году Жозефа Гай-Люссака и Луи Жакана открыли бром и йод.
- В 1856 году русский химик Станислав Канторович открыл родий.
- В 1925 году американский физик Джордж Пагерт Тайлер создал первый искусственный элемент — польоний.
Это лишь некоторые примеры открытий химических элементов, которые внесли значительный вклад в науку и привели к расширению и совершенствованию периодической системы.
Открытие новых элементов имеет большое значение для развития химии и науки в целом. Каждый новый элемент даёт ученым новые возможности для исследования и понимания природы вещества.
Попытки создать систематическую классификацию
С момента открытия первых элементов были предприняты различные попытки создать систематическую классификацию химических элементов. Однако, данные системы не были полными и не удовлетворяли всем требованиям.
Первая попытка создать систему классификации была предпринята Гансом Хайнрихом Регельманном в 1789 году. Он разделил элементы на металлы и неметаллы и классифицировал их по химическим свойствам. Эта система была несовершенна и не позволяла предсказывать свойства новых элементов.
Более точные попытки создать систематическую классификацию были предприняты в XIX веке, особенно после открытия множества новых элементов. Одним из важных этапов в развитии классификации элементов была работа Менделеева.
Дмитрий Иванович Менделеев в 1869 году предложил периодическую систему химических элементов, основанную на периодическом законе. Эта система отражала взаимосвязь между атомными массами и химическими свойствами элементов и позволяла предсказывать свойства новых элементов. Периодическая система Менделеева получила широкое признание и стала основой для дальнейшего развития химии и физики.
С течением времени было открыто все больше новых элементов и периодическая система была совершеюща. Она претерпевала изменения и уточнения, но оставалась надежной основой для классификации элементов.
| Период | Группа 1 | Группа 2 | … | Группа 18 | ||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 1 | H | Li | … | He | ||||||||||||||
| 2 | Be | B | … | Ne | ||||||||||||||
| … | … | … | … | … | ||||||||||||||
| 7 | Rb | … | Fr | |||||||||||||||
В таблице выше приведена современная периодическая система химических элементов, которая основана на работе Менделеева. Каждый элемент имеет свою уникальную атомную массу и расположен в соответствующей группе и периоде.
Строение и принципы
Периодическая система химических элементов представляет собой упорядоченную таблицу, где элементы располагаются в порядке возрастания атомного номера. Она состоит из горизонтальных строк, называемых периодами, и вертикальных столбцов, называемых группами. Каждый элемент химической системы представлен своим символом и атомным номером.
Основной принцип периодической системы заключается в том, что элементы, расположенные в одной группе (вертикально), имеют схожие химические свойства и обладают схожей электронной конфигурацией. Это обусловлено тем, что элементы в одной группе имеют одинаковое количество электронов во внешней электронной оболочке.
Кроме того, периодическая система Менделеева представляет элементы в порядке возрастания их атомных номеров. Атомный номер элемента определяет количество протонов в ядре и электронов в атоме. В таблице элементы упорядочены по возрастанию атомных номеров, начиная с водорода (атомный номер 1) и заканчивая оганесоном (атомный номер 118).
Периодическая система химических элементов является ключевым инструментом в изучении химии. Она позволяет систематизировать и классифицировать элементы, а также предсказывать их свойства на основе их положения в таблице. Эта система обладает огромной значимостью для развития химической науки и применения ее в различных областях жизни человека.
Основные элементы и группы
В ПСХЭ элементы разделены на различные группы по их общим свойствам и химическим характеристикам. Одной из ключевых особенностей ПСХЭ является периодический закон, согласно которому химические и физические свойства элементов меняются периодически с увеличением их атомного номера.
Основные элементы — это элементы, составляющие большую часть Менделеевской таблицы. Они также называются макроэлементами, и включают в себя такие химические элементы, как кислород, углерод, водород и азот. Эти элементы являются основными строительными блоками живых организмов и имеют важное значение для жизненных процессов.
Группы элементов в ПСХЭ обозначаются числами от 1 до 18. Каждая группа имеет свои характерные свойства и образует вертикальные столбцы в таблице. Например, первая группа представлена элементами алкалий, вторая — щелочноземельными металлами, седьмая — галогенами, а восьмая — инертными газами.
Каждый элемент в ПСХЭ обозначается символом (обычно, из одной или двух латинских букв) и атомным номером. Например, кислород обозначается символом «O» и имеет атомный номер 8. Кроме этого, в таблице указывается относительная атомная масса каждого элемента.
Ознакомление с ПСХЭ и основными элементами и группами помогает лучше понять химические свойства и взаимодействие различных веществ, а также имеет практическое применение в различных областях науки, техники и промышленности.
Периоды и блоки
Периодическая система химических элементов состоит из 7 горизонтальных строк, называемых периодами. Каждый период представляет собой новый энергетический уровень, на котором находятся электроны. Элементы в периоде имеют одинаковое количество энергетических уровней, а значит, электроны находятся на одном и том же расстоянии от ядра.
Всего в периодической системе 18 вертикальных столбцов, называемых блоками. Блоки группируют элементы схожих химических свойств и электронной конфигурации. В блоках можно выделить несколько основных групп:
- С-блок: состоит из двух частей — группы 1 и 2, которые называют щелочными и щелочноземельными металлами соответственно. Элементы в данном блоке обладают низкой электроотрицательностью и хорошо реагируют с другими веществами.
- Р-блок: состоит из групп 3-12 и называется блоком переходных металлов. Эти элементы имеют переменную степень окисления и обладают высокими плотностью и температурой плавления.
- D-блок: состоит из элементов с атомными номерами от 21 до 30, 39 до 48, 57 до 80 и 89 до 112. Эти элементы также относятся к переходным металлам, но имеют особенности в электронной конфигурации и химических свойствах.
- Ф-блок: состоит из лантаноидов и актиноидов, которые расположены под таблицей. Эти элементы имеют схожие электронные конфигурации и химические свойства.
Знание о блоках и периодах помогает в идентификации элементов и их химических свойств, а также использовании периодической системы для прогнозирования свойств еще неизвестных элементов.
Расположение элементов в таблице
Горизонтальными строками таблицы являются периоды. Первый период содержит только 2 элемента — водород и гелий. Второй период содержит 8 элементов, третий — 8 элементов, четвертый — 18 элементов, пятый — 18 элементов, шестой — 32 элемента, седьмой — 32 элемента, восьмой — 18 элементов, а девятый — 18 элементов.
Вертикальными столбцами таблицы являются группы. В каждой группе находятся элементы, имеющие одинаковое число валентных электронов во внешней оболочке. Первая группа состоит из элементов с одним валентным электроном, вторая — из элементов с двумя валентными электронами и так далее. Восьмая группа, также называемая инертными газами, содержит элементы, у которых полностью заполнена внешняя оболочка и необходимо указывать их валентность как 0.
В таблице периодической системы химических элементов также выделяются блоки элементов: s-блок, p-блок, d-блок и f-блок. S-блок расположен слева в таблице и состоит из элементов с небольшим числом электронов в оболочке. P-блок находится в центре таблицы и содержит элементы с заполненными s-оболочками и внешними p-оболочками. D-блок состоит из переходных металлов, располагается между s-блоком и p-блоком. F-блок, самый большой блок, расположен под основной таблицей и содержит элементы из внутреннего переходного ряда.
Расположение элементов в таблице периодической системы позволяет увидеть закономерности и связи между элементами. Оно также дает представление об электронной структуре элементов и их химических свойствах.
Практическое применение
Периодическая система химических элементов и периодический закон Менделеева имеют широкое практическое применение во многих областях науки и технологий.
Химическая промышленность: Периодическая система помогает установить связь между свойствами элементов и их расположением в таблице. Это позволяет разрабатывать новые материалы и вещества, оптимизировать процессы синтеза и прогнозировать их свойства.
Энергетика: Периодическая система используется в разработке и улучшении материалов для энергетических установок, таких как солнечные панели, батарейки и ядерные реакторы. Знание химических элементов позволяет определить оптимальные условия эксплуатации и выбрать наиболее эффективные материалы для хранения и передачи энергии.
Медицина: Периодическая система помогает в изучении биохимических процессов, идущих в организме и взаимодействии лекарств с тканями. Она также используется в разработке новых препаратов, диагностических методик и инструментов для лечения различных заболеваний.
Электроника: Знание периодической системы позволяет создавать новые материалы для электронных компонентов, таких как полупроводники и проводящие материалы. Это помогает повысить эффективность и мощность электронных устройств, уменьшить их размеры и повысить надежность работы.
Экология: Периодическая система помогает анализировать загрязнение окружающей среды и прогнозировать его последствия. Она также используется для разработки методов очистки воды, воздуха и почвы от загрязняющих веществ.
Вопрос-ответ:
Как была создана периодическая система химических элементов?
Периодическая система химических элементов была создана российским химиком Дмитрием Ивановичем Менделеевым в 1869 году. Он систематизировал известные на тот момент химические элементы по возрастанию их атомных масс и расположил их в таблице. Менделеев учел множество химических и физических свойств элементов и оставил пустые места в таблице для элементов, которые он предсказал. Его система стала основой для современной периодической системы.
Какие данные учитывались для создания периодической системы Менделеева?
Для создания периодической системы Менделеев учел множество данных, включая атомные массы, химические свойства и плотности элементов. Он также учитывал закономерности, которые наблюдались в химических реакциях элементов и предсказал свойства новых элементов, которые были открыты позже. Менделеев исследовал множество свойств элементов и использовал эти данные, чтобы создать логическую и систематическую таблицу элементов.
Какие элементы Менделеев предсказал и как он их описал?
Менделеев предсказал существование нескольких элементов, которые еще не были открыты на момент создания его периодической системы. Он оставил пустые места в таблице для этих элементов, а также указал их предполагаемые свойства. Некоторые из предсказанных Менделеевым элементов были галлий, германий и скандий. Он описал эти элементы на основе закономерностей, которые он обнаружил в таблице и свойствах соседних элементов. Позднее эти элементы были открыты и подтвердили предсказания Менделеева.
Какой вклад в развитие периодической системы химических элементов внес Дмитрий Иванович Менделеев?
Дмитрий Иванович Менделеев сделал уникальный вклад в развитие периодической системы химических элементов. Он предложил упорядочить элементы по возрастанию атомных масс и сгруппировать их по сходству свойств. Менделеев также предсказал существование некоторых элементов и оставил пустые места в таблице, которые были заполнены впоследствии открытыми новыми элементами. Его работа является одним из ключевых достижений в области химии и играет важную роль в современной науке и промышленности.